阿尔茨海默病,也是我们常说的“老年痴呆症”,就像大脑被按下了倒退的开关——上了年纪的人可能突然记不起回家的路,认不出朝夕相处的亲人,甚至连日常吃穿都变得困难。这种病本质上是一种中枢神经系统的“退行性故障”,患者会逐渐出现认知功能障碍和行为异常。目前,相关治疗研究大多聚焦于清除大脑内的β淀粉样蛋白(Aβ)沉积,但药物的开发仍面临诸多挑战和困难。
近日,深圳华大生命科学研究院联合西北农林科技大学在国际学术期刊《阿尔茨海默氏症与痴呆症》(Alzheimer's & Dementia)发表研究,首次发现肠道影响大脑抗炎机制的关键——肠道菌群代谢物吲哚乳酸,并验证了靶向干预策略的有效性,为阿尔兹海默病的预防与治疗带来新曙光。
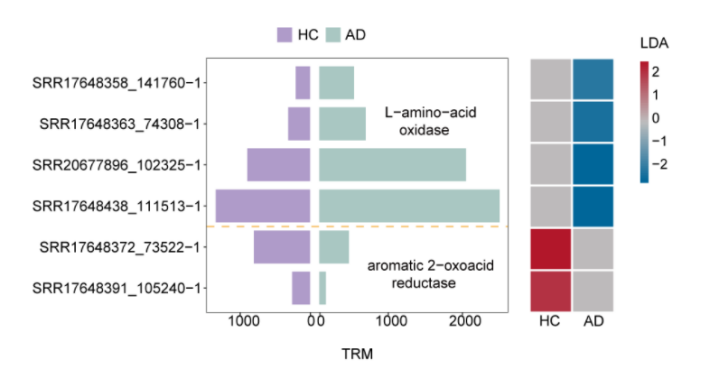
Alzheimer's & Dementia官网截图研究团队通过分析164名临床前阿尔茨海默病患者与健康人的肠道菌群宏基因组数据,发现患者体内的吲哚乳酸(ILA)合成通路活性显著下调。ILA是一种由色氨酸代谢产生的小分子物质,不仅是肠道菌群的重要信号分子,更在本研究中被证实能穿透血脑屏障,直接影响大脑的神经炎症水平。
“打个比方,这就像是肠道向大脑发送的加密电报信号被中断了。”文章通讯作者、深圳华大生命科学研究院邹远强博士解释道,“ILA水平的下降,可能使大脑失去一种关键的抗炎保护机制。”
研究团队通过开展动物实验,进一步证实了这一发现。研究结果显示,与健康小鼠相比,阿尔茨海默病模型小鼠的粪便和血清中ILA浓度显著降低,同时脑部Aβ蛋白沉积量与脑部神经炎症程度则显著增加。
AD:临床前阿尔茨海默病患者;HC:健康对照
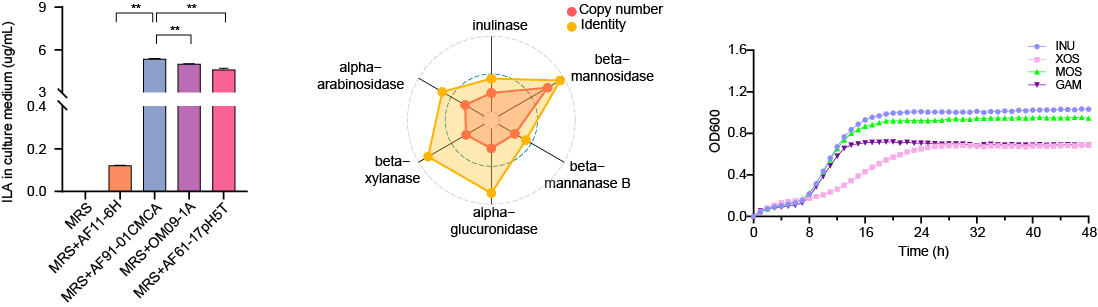
为了探索靶向提升ILA的干预策略,研究团队依托华大生命科学研究院前期构建的“中国健康人群肠道微生物菌株资源库(CGR2)”,深入分析了ILA合成通路,筛选出23株具有潜在ILA生产能力的肠道益生菌。其中,预测有4株菌能独立将色氨酸代谢生成ILA。随后的体外实验发现,绥宁乳杆菌生产ILA的能力显著高于其它候选菌株,因此被选定为目标菌株。
华大生命科学研究院宏基因组研究团队长期致力于人体微生物菌株资源库的构建,先后在《自然·生物技术》和《自然·通讯》发表文章,累计构建超6万株人体共生微生物的菌株库,为人体微生物体外功能的研究、益生菌等功能产物的挖掘等提供了宝贵的基础资源和数据。
此外,研究团队在阿尔茨海默病小鼠模型上进行了干预实验。结果显示,补充绥宁乳杆菌后,能够对5×FAD转基因阿尔茨海默病模型小鼠(携带5个家族性基因突变的APP/PS1转基因小鼠)的脑部神经炎症和Aβ蛋白沉积产生一定的改善作用,且干预组小鼠脑部的炎症因子浓度显著降低。随后,研究团队探索了将益生菌与益生元菊粉搭配使用的效果。菊粉是一种优质的天然水溶性膳食纤维,被认为具有调节肠道菌群的功能,能为益生菌提供专属“营养餐”。
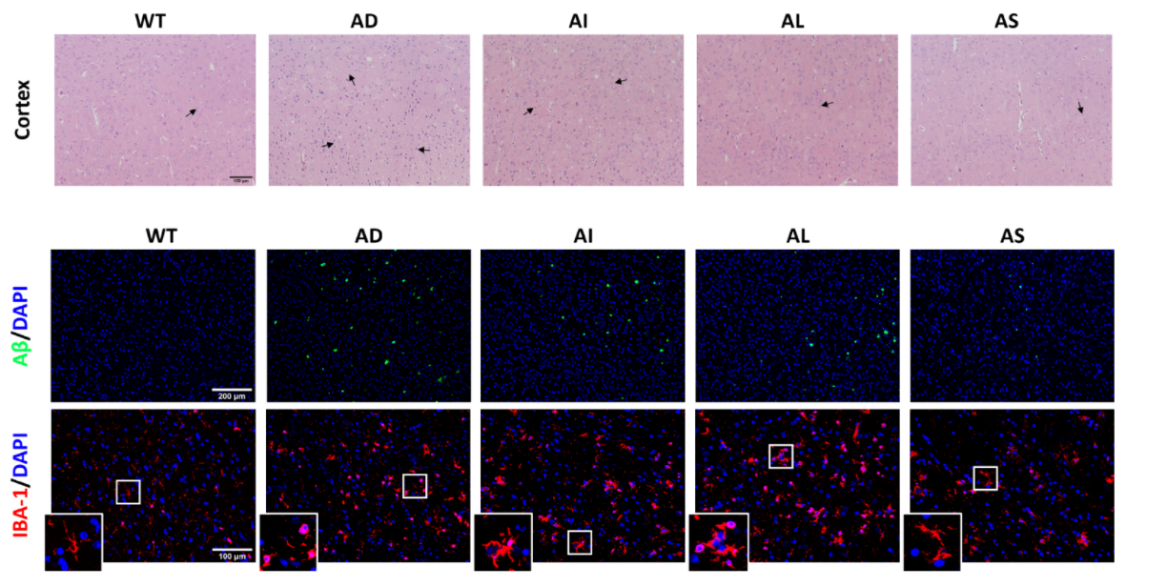
在5×FAD转基因阿尔茨海默病模型小鼠中,使用绥宁乳杆菌搭配菊粉进行干预后,肠道及血清中的ILA水平得到了显著提升。更令人欣喜的是,组合干预的效果显著优于单独使用益生菌:小鼠脑部的Aβ蛋白沉积量、活化的小胶质细胞数量以及促炎因子浓度均出现更大幅度的下降;并且,在迷宫行为测试中也展现出接近正常小鼠水平的空间记忆能力。
深入的机制研究表明,ILA通过激活芳香烃受体信号通路,显著抑制了脑部小胶质细胞的过度活化,并显著降低了Aβ蛋白的沉积,从而阻断了“神经炎症-神经元损伤”的恶性循环。
小鼠大脑皮质图像
本项研究不仅揭示了ILA水平与阿尔茨海默病发生、发展的密切关联,证实了肠道细菌通过特定代谢产物对脑部神经健康状态的影响,更为相关的临床转化和干预应用提供了潜在方向:
1、早筛新指标:ILA或成为阿尔茨海默病早期筛查的生物标志物,助力精准诊断;
2、治疗新方案:首款针对肠道色氨酸代谢的合生制剂(益生菌与益生元结合)雏形诞生;
3、预防新策略:选择合生元进行日常防护,或可成为预防阿尔茨海默病的新选择。
或许在不远的未来,我们能够从肠道入手,以新一代益生菌和益生元的组合搭配,为脑神经系统筑起一道抵御阿尔茨海默病的防线。这场始于肠道的科学革命,有可能刷新对于神经退行性疾病的预防、干预认知。 西北农林科技大学刘志刚教授、深圳华大生命科学研究院邹远强研究员为本文的共同通讯作者。西北农林科技大学硕士研究生杨聪、中国科学院大学-深圳华大生命科学研究院联合培养硕士研究生孙菁希、西北农林科技大学博士研究生李铃为本论文共同第一作者。本研究已通过伦理和人遗审查,严格遵循相应法规和伦理准则。